IUPAC नामकरण, हिंदी में
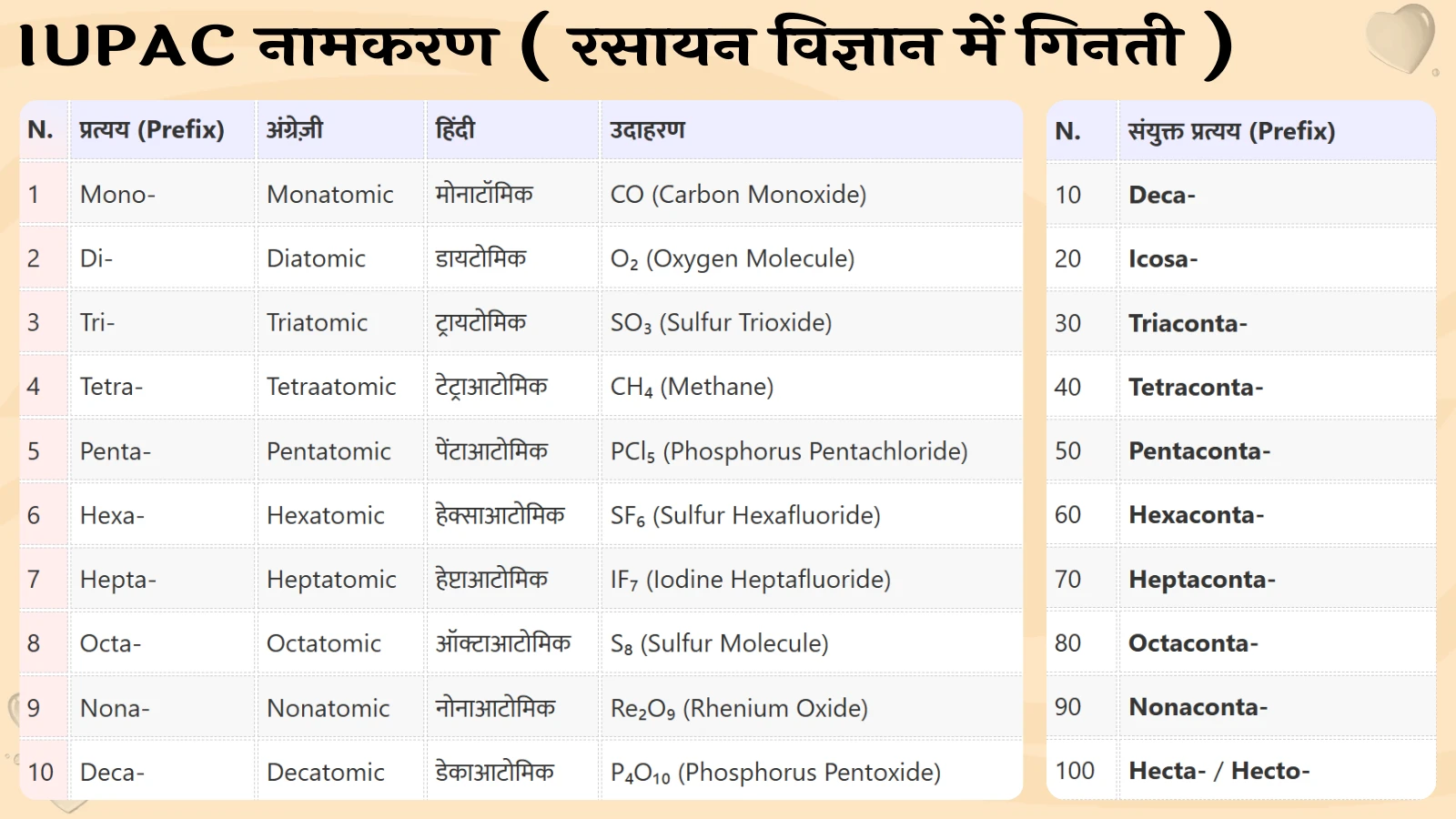
IUPAC (International Union of Pure and Applied Chemistry) रसायन विज्ञान में नामकरण के लिए अंतर्राष्ट्रीय प्रणाली प्रदान करता है। इसमें संख्यात्मक शब्दों (Numerical Terms) का उपयोग रासायनिक यौगिकों में परमाणुओं (Atoms) या समूहों (Groups) की संख्या को दर्शाने के लिए किया जाता है। ये शब्द ग्रीक मूल के होते हैं और संयुक्त प्रत्यय (Prefixes) के रूप में प्रयुक्त होते हैं।
रसायन विज्ञान में गिनती (काउंटिंग):
| N. | संयुक्त प्रत्यय (Prefix) | अंग्रेज़ी | हिंदी | उदाहरण |
|---|---|---|---|---|
| 1 | Mono (मोनो)- | Monatomic | मोनाटॉमिक | CO (Carbon Monoxide) |
| 2 | Di (डाई)- | Diatomic | डायटोमिक | O₂ (Oxygen Molecule) |
| 3 | Tri (ट्राई)- | Triatomic | ट्रायटोमिक | SO₃ (Sulfur Trioxide) |
| 4 | Tetra (टेट्रा)- | Tetraatomic | टेट्राआटोमिक | CH₄ (Methane) |
| 5 | Penta (पेन्टा)- | Pentatomic | पेंटाआटोमिक | PCl₅ (Phosphorus Pentachloride) |
| 6 | Hexa (हेक्सा)- | Hexatomic | हेक्साआटोमिक | SF₆ (Sulfur Hexafluoride) |
| 7 | Hepta (हेप्टा)- | Heptatomic | हेप्टाआटोमिक | IF₇ (Iodine Heptafluoride) |
| 8 | Octa (ओक्टा)- | Octatomic | ऑक्टाआटोमिक | S₈ (Sulfur Molecule) |
| 9 | Nona (नोना)- | Nonatomic | नोनाआटोमिक | Re₂O₉ (Rhenium Oxide) |
| 10 | Deca (डेका)- | Decatomic | डेकाआटोमिक | P₄O₁₀ (Phosphorus Pentoxide) |
नोट:
- यह संयुक्त प्रत्यय (Prefix) आमतौर पर रासायनिक यौगिकों (Chemical Compounds) में परमाणुओं (Atoms) की संख्या दर्शाने के लिए उपयोग किए जाते हैं।
- ग्रीक संख्यात्मक प्रत्ययों का उपयोग आणविक यौगिकों (Molecular Compounds) के नामकरण में किया जाता है।
IUPAC संख्यात्मक प्रत्यय (Numerical Prefixes) सारणी
| N. | संयुक्त प्रत्यय (Prefix) | उदाहरण (Example) |
|---|---|---|
| 1 | Mono (मोनो)- | CO (Carbon Monoxide) |
| 2 | Di (डाई)- | NO₂ (Nitrogen Dioxide) |
| 3 | Tri (ट्राई)- | SO₃ (Sulfur Trioxide) |
| 4 | Tetra (टेट्रा)- | CCl₄ (Carbon Tetrachloride) |
| 5 | Penta (पेन्टा)- | PCl₅ (Phosphorus Pentachloride) |
| 6 | Hexa (हेक्सा)- | SF₆ (Sulfur Hexafluoride) |
| 7 | Hepta (हेप्टा)- | IF₇ (Iodine Heptafluoride) |
| 8 | Octa (ओक्टा)- | OsO₈ (Osmium Tetroxide) |
| 9 | Nona (नोना)- | Re₂O₉ (Rhenium Oxide) |
| 10 | Deca (डेका)- | P₄O₁₀ (Phosphorus Pentoxide) |
IUPAC नामकरण में उपयोग:
- मोनो (Mono-) केवल दूसरे तत्व के साथ उपयोग किया जाता है। (उदा: CO = Carbon Monoxide, न कि Carbon Monooxide)
- ये संयुक्त प्रत्यय (Prefixes) मुख्य रूप से आणविक यौगिकों (Molecular Compounds) में प्रयुक्त होते हैं।
- धातु-मिश्र धातु (Alloys) और अकार्बनिक यौगिकों के नामकरण में इनका उपयोग कम होता है।
उदाहरण:
- N₂O₅ → Dinitrogen Pentoxide
- P₄O₁₀ → Tetraphosphorus Decoxide
बड़े और जटिल यौगिक के लिए संख्यात्मक संयुक्त प्रत्यय:
| N. | संयुक्त प्रत्यय (Prefix) |
|---|---|
| 10 | Deca- |
| 20 | Icosa- |
| 30 | Triaconta- |
| 40 | Tetraconta- |
| 50 | Pentaconta- |
| 60 | Hexaconta- |
| 70 | Heptaconta- |
| 80 | Octaconta- |
| 90 | Nonaconta- |
| 100 | Hecta- / Hecto- |
| 200 | Dicta- / Dichecta- |
| 300 | Tricta- / Trichecta- |
| 400 | Tetracta- / Tetrachecta- |
| 500 | Pentacta- / Pentachecta- |
| 600 | Hexacta- / Hexachecta- |
| 700 | Heptacta- / Heptachecta- |
| 800 | Octacta- / Octachecta- |
| 900 | Nonacta- / Nonachecta- |
| 1000 | Kilia- / Chilia- |
| 2000 | Dichilia- |
| 3000 | Trichilia- |
| 4000 | Tetrachilia- |
| 5000 | Pentachilia- |
| 6000 | Hexachilia- |
| 7000 | Heptachilia- |
| 8000 | Octachilia- |
| 9000 | Nonachilia- |
IUPAC नामकरण में उपयोग:
- 30 से 90 तक के लिए
-contaप्रत्यय का प्रयोग किया जाता है। - 100 से 900 तक के लिए
-ctaया-chectaप्रत्यय का उपयोग होता है। - 1000 से अधिक के लिए
-chiliaप्रत्यय का प्रयोग किया जाता है।
IUPAC नाम उदाहरण:
- C₁₀H₂₂ → Decane (10 कार्बन परमाणु)
- C₂₀H₄₂ → Icosaane (20 कार्बन परमाणु)
- C₁₀₀H₂₀₂ → Hectane (100 कार्बन परमाणु)
- C₁₀₀₀H₂₀₀₂ → Kiliaane (1000 कार्बन परमाणु)
IUPAC नाम कैसे लिखें?
IUPAC (International Union of Pure and Applied Chemistry) द्वारा विकसित नामकरण प्रणाली का उपयोग रासायनिक यौगिकों के सही और मानकीकृत नामकरण के लिए किया जाता है। नीचे IUPAC नाम लिखने के स्टेप-बाय-स्टेप नियम दिए गए हैं।
कार्बन श्रृंखला
- उस सबसे लंबी लगातार कार्बन श्रृंखला को खोजें, जिसमें प्रमुख कार्यात्मक समूह (Functional Group) या यौगिक की विशेषता मौजूद हो।
- यदि एक से अधिक सबसे लंबी श्रृंखला संभव हो, तो वह चुनें जिसमें सबसे ज्यादा कार्यात्मक समूह या उपसमूह (Substituent) हों।
उदाहरण:
अगर हमारे पास यह संरचना है:
CH₃-CH₂-CH₂-CH₃
- यह 4 कार्बन वाली श्रृंखला है, इसलिए इसका मूल नाम Butane (ब्यूटेन) होगा।
नंबरिंग (Numbering the Chain)
- मुख्य श्रृंखला में सबसे महत्वपूर्ण कार्यात्मक समूह को सबसे छोटा नंबर देने के लिए बाएँ से या दाएँ से नंबरिंग करें।
- यदि कोई कार्यात्मक समूह न हो, तो पहला उपसमूह (Substituent) कम से कम नंबर पर आए।
- यदि दो अलग-अलग उपसमूह हैं, तो उन्हें वर्णानुक्रम (Alphabetical Order) में लिखें।
उदाहरण:
CH₃
|
CH₃-CH-CH₂-CH₃
- सबसे लंबी श्रृंखला 4 कार्बन वाली है, और CH₃ (Methyl Group) को सबसे कम संख्या (2) पर देना सही रहेगा।
- IUPAC नाम: 2-Methylbutane (2-मिथाइलब्यूटेन)
कार्यात्मक समूह (Functional Group)
- कार्यात्मक समूह (Functional Group) यौगिक की मुख्य विशेषता निर्धारित करता है।
- कार्यात्मक समूह को पहचानने के बाद, इसे प्राथमिकता के आधार पर सबसे छोटे नंबर पर रखें।
- कार्यात्मक समूह के लिए IUPAC प्रत्यय (Suffix) लगाएँ।
प्रमुख कार्यात्मक समूह और उनके प्रत्यय:
| कार्यात्मक समूह | संरचना | प्रत्यय (Suffix) | उदाहरण | IUPAC नाम |
|---|---|---|---|---|
| अल्केन (Alkane) | C-C | -ane | CH₄ | Methane |
| अल्कीन (Alkene) | C=C | -ene | C₂H₄ | Ethene |
| अल्काइन (Alkyne) | C≡C | -yne | C₂H₂ | Ethyne |
| अल्कोहल (Alcohol) | -OH | -ol | CH₃OH | Methanol |
| कार्बोक्सिलिक अम्ल (Carboxylic Acid) | -COOH | -oic acid | CH₃COOH | Ethanoic Acid |
| कीटोन (Ketone) | >C=O | -one | CH₃COCH₃ | Propanone |
| ऐल्डिहाइड (Aldehyde) | -CHO | -al | CH₃CHO | Ethanal |
| ईथर (Ether) | -O- | ether | CH₃-O-CH₃ | Dimethyl Ether |
| अमीन (Amine) | -NH₂ | -amine | CH₃NH₂ | Methylamine |
उपसमूह (Substituents)
- यदि कोई अतिरिक्त उपसमूह (जैसे मिथाइल -CH₃, एथाइल -C₂H₅) मौजूद हो, तो उन्हें वर्णानुक्रम (Alphabetical Order) में लिखें।
- उपसमूह के स्थान को संख्या द्वारा दर्शाया जाता है।
- यदि एक ही प्रकार का उपसमूह बार-बार आता है, तो Di (2), Tri (3), Tetra (4) जैसे उपसर्ग लगाएँ।
उदाहरण:
CH₃
|
CH₃-CH-CH-CH₃
|
CH₃
- यहाँ दो मिथाइल (-CH₃) समूह हैं, जो दूसरे और तीसरे कार्बन पर जुड़े हैं।
- IUPAC नाम: 2,3-Dimethylbutane (2,3-डाइमेथाइलब्यूटेन)
उदाहरण
CH₃-CH(OH)-CH₂-CH₃
- सबसे लंबी श्रृंखला 4 कार्बन वाली (Butane) है।
- -OH (Alcohol) समूह प्राथमिक कार्यात्मक समूह है, इसलिए “ol” प्रत्यय लगेगा।
- OH को सबसे छोटा नंबर (2) दें।
- IUPAC नाम: 2-Butanol (2-ब्यूटेनॉल)
अल्केन, अल्कीन और अल्काइन में अंतर
| प्रकार | बंधों की संख्या | नामकरण | उदाहरण |
|---|---|---|---|
| एल्केन (Alkane) | केवल एकल बंध (Single Bond) | -ane प्रत्यय | Methane (CH₄), Ethane (C₂H₆) |
| एल्कीन (Alkene) | कम से कम एक डबल बंध (Double Bond) | -ene प्रत्यय | Ethene (C₂H₄), Propene (C₃H₆) |
| एल्काइन (Alkyne) | कम से कम एक ट्रिपल बंध (Triple Bond) | -yne प्रत्यय | Ethyne (C₂H₂), Propyne (C₃H₄) |
एल्केन (Alkane)
एल्केन (Alkane) हाइड्रोकार्बन (Hydrocarbon) का एक मुख्य वर्ग है, जिसमें केवल कार्बन (C) और हाइड्रोजन (H) परमाणु मौजूद होते हैं। यह संतृप्त हाइड्रोकार्बन (Saturated Hydrocarbon) होते हैं, क्योंकि इनमें सभी कार्बन-कार्बन बंध एकल (Single) बंध होते हैं। एल्केन का सामान्य मोलिक्यूलर सूत्र CₙH₂ₙ₊₂ होता है।
एल्केन की पहचान के लिए निम्नलिखित विशेषताओं को देखें:
- सूत्र: यदि किसी यौगिक का CₙH₂ₙ₊₂ से मेल खाता है, तो वह एल्केन हो सकता है।
- एकल बंध (Single Bond): एल्केन में केवल σ-बॉन्ड (Sigma Bond) होते हैं, कोई डबल (C=C) या ट्रिपल (C≡C) बंध नहीं होता।
- जल में अघुलनशील: ये जल में नहीं घुलते, लेकिन कार्बनिक विलायकों (Organic Solvents) में घुल सकते हैं।
- दहन (Combustion) प्रतिक्रिया: एल्केन हवा में जलने पर कार्बन डाइऑक्साइड (CO₂) और पानी (H₂O) बनाते हैं।
- IUPAC नामकरण: एल्केन के नाम में अंत में “-ane” प्रत्यय होता है, जैसे Methane (CH₄), Ethane (C₂H₆), Propane (C₃H₈) आदि।
एल्केन (Alkane) उदाहरण:
- Methane (CH₄) – सबसे सरल एल्केन
- Butane (C₄H₁₀) – LPG का मुख्य घटक
- Octane (C₈H₁₈) – पेट्रोल का महत्वपूर्ण घटक
एल्केन ऊर्जा के मुख्य स्रोतों में से एक हैं और ईंधन, गैस, प्लास्टिक और रसायनों के उत्पादन में उपयोग किए जाते हैं।
एल्केन (Alkane) कार्बन परमाणु कार्बन परमाणु उपसर्ग तालिका:
| N. | उपसर्ग (Prefix) | हिंदी | उदाहरण (Example – Alkane) | संरचना (Formula) |
|---|---|---|---|---|
| 1 | Meth- | मीथ- | Methane (मीथेन) | CH₄ |
| 2 | Eth- | एथ- | Ethane (एथेन) | C₂H₆ |
| 3 | Prop- | प्रोप- | Propane (प्रोपेन) | C₃H₈ |
| 4 | But- | ब्यूट- | Butane (ब्यूटेन) | C₄H₁₀ |
| 5 | Pent- | पेंट- | Pentane (पेंटेन) | C₅H₁₂ |
| 6 | Hex- | हेक्स- | Hexane (हेक्सेन) | C₆H₁₄ |
| 7 | Hept- | हेप्ट- | Heptane (हेप्टेन) | C₇H₁₆ |
| 8 | Oct- | ऑक्ट- | Octane (ऑक्टेन) | C₈H₁₈ |
| 9 | Non- | नॉन- | Nonane (नॉनैन) | C₉H₂₀ |
| 10 | Dec- | डेक- | Decane (डेकैन) | C₁₀H₂₂ |
| 11 | Undec- | अनडेक- | Undecane (अनडेकैन) | C₁₁H₂₄ |
| 12 | Dodec- | डोडेक- | Dodecane (डोडेकैन) | C₁₂H₂₆ |
| 13 | Tridec- | ट्राइडेक- | Tridecane (ट्राइडेकैन) | C₁₃H₂₈ |
| 14 | Tetradec- | टेट्राडेक- | Tetradecane (टेट्राडेकैन) | C₁₄H₃₀ |
| 15 | Pentadec- | पेंटाडेक- | Pentadecane (पेंटाडेकैन) | C₁₅H₃₂ |
| 16 | Hexadec- | हेक्साडेक- | Hexadecane (हेक्साडेकैन) | C₁₆H₃₄ |
| 17 | Heptadec- | हेप्टाडेक- | Heptadecane (हेप्टाडेकैन) | C₁₇H₃₆ |
| 18 | Octadec- | ऑक्टाडेक- | Octadecane (ऑक्टाडेकैन) | C₁₈H₃₈ |
| 19 | Nonadec- | नोनाडेक- | Nonadecane (नोनाडेकैन) | C₁₉H₄₀ |
| 20 | Icos- | आईकोस- | Icosane (आईकोसैन) | C₂₀H₄₂ |
| 21 | Henicos- | हेनिकोज- | Henicosane (हेनिकोज़ैन) | C₂₁H₄₄ |
| 22 | Docos- | डोकोस- | Docosane (डोकोसैन) | C₂₂H₄₆ |
| 23 | Tricos- | ट्राईकोस- | Tricosane (ट्राईकोसैन) | C₂₃H₄₈ |
| 24 | Tetracos- | टेट्राकोस- | Tetracosane (टेट्राकोसैन) | C₂₄H₅₀ |
| 25 | Pentacos- | पेंटाकोस- | Pentacosane (पेंटाकोसैन) | C₂₅H₅₂ |
| 26 | Hexacos- | हेक्साकोस- | Hexacosane (हेक्साकोसैन) | C₂₆H₅₄ |
| 27 | Heptacos- | हेप्टाकोस- | Heptacosane (हेप्टाकोसैन) | C₂₇H₅₆ |
| 28 | Octacos- | ऑक्टाकोस- | Octacosane (ऑक्टाकोसैन) | C₂₈H₅₈ |
| 29 | Nonacos- | नोनाकोस- | Nonacosane (नोनाकोसैन) | C₂₉H₆₀ |
| 30 | Triacont- | ट्रायाकोंट- | Triacontane (ट्रायाकोंटेन) | C₃₀H₆₂ |
एल्केन (Alkane) के गुण और पहचान
एल्केन (Alkane) संतृप्त हाइड्रोकार्बन (Saturated Hydrocarbon) होते हैं, जिनमें केवल कार्बन-कार्बन (C-C) एकल बंध (Single Bond) मौजूद होते हैं। इनका सामान्य सूत्र CₙH₂ₙ₊₂ होता है। एल्केन प्राकृतिक गैस, पेट्रोलियम और ईंधन स्रोतों का एक प्रमुख घटक होते हैं।
- संरचना: केवल σ-बॉन्ड (Sigma Bond) होते हैं, कोई डबल (C=C) या ट्रिपल (C≡C) बंध नहीं होता।
- सूत्र: यदि किसी यौगिक का CₙH₂ₙ₊₂ से मेल खाता है, तो वह एल्केन हो सकता है।
- जल में अघुलनशील: ये जल में नहीं घुलते, लेकिन कार्बनिक विलायकों (Organic Solvents) में घुल सकते हैं।
- अपारंभिक (Non-Polar): एल्केन गैर-ध्रुवीय (Non-Polar) अणु होते हैं, इसलिए ये जल में घुलते नहीं हैं।
- दहन (Combustion) प्रतिक्रिया: हवा में जलने पर कार्बन डाइऑक्साइड (CO₂) और पानी (H₂O) का उत्पादन करते हैं।
- IUPAC नामकरण: एल्केन के नाम के अंत में “-ane” प्रत्यय होता है, जैसे Methane (CH₄), Ethane (C₂H₆), Propane (C₃H₈) आदि।
Alkane (एल्केन) यौगिकों के नियम:
- कार्बन परमाणुओं की संख्या के अनुसार उपसर्ग (Prefix) का प्रयोग किया जाता है।
- नाम के अंत में “-ane” (एन) प्रत्यय जोड़ा जाता है।
- सामान्य सूत्र CₙH₂ₙ₊₂ का पालन किया जाता है।
एल्केन यौगिकों उदाहरण:
- C₁₀H₂₂ → Decane (डेकैन)
- C₂₀H₄₂ → Icosane (आईकोसैन)
- C₃₀H₆₂ → Triacontane (ट्रायाकोंटेन)
एल्कीन (Alkene)
एल्कीन (Alkene) हाइड्रोकार्बन (Hydrocarbon) का एक मुख्य वर्ग है, जिसमें कार्बन (C) और हाइड्रोजन (H) परमाणु मौजूद होते हैं। यह असंतृप्त हाइड्रोकार्बन (Unsaturated Hydrocarbon) होते हैं, क्योंकि इनमें कम से कम एक कार्बन-कार्बन डबल (C=C) बंध मौजूद होता है। एल्कीन का सामान्य मोलिक्यूलर सूत्र CₙH₂ₙ होता है।
एल्कीन की पहचान के लिए निम्नलिखित विशेषताओं को देखें:
- सूत्र: यदि किसी यौगिक का CₙH₂ₙ से मेल खाता है, तो वह एल्कीन हो सकता है।
- डबल बंध (Double Bond): एल्कीन में कम से कम एक C=C (डबल बंध) मौजूद होता है, जो इसे एल्केन से अलग बनाता है।
- π-बॉन्ड (Pi Bond) मौजूद होता है, जो इसे अधिक प्रतिक्रियाशील (Reactive) बनाता है।
- जोड़ने की प्रतिक्रिया (Addition Reaction) जैसे हाइड्रोजनीकरण (Hydrogenation), हलोजन जुड़ाव (Halogenation), हाइड्रेशन (Hydration) आदि में भाग लेते हैं।
- ब्रॉमीन जल परीक्षण (Bromine Water Test): ब्रॉमीन जल (Br₂ Water) का रंग एल्कीन के साथ प्रतिक्रिया करने पर फीका पड़ जाता है, जबकि एल्केन के साथ ऐसा नहीं होता।
- IUPAC नामकरण: एल्कीन के नाम में अंत में “-ene” प्रत्यय होता है, जैसे Ethene (C₂H₄), Propene (C₃H₆), Butene (C₄H₈) आदि।
एल्कीन औद्योगिक रसायन, प्लास्टिक, दवाओं और ईंधन के निर्माण में महत्वपूर्ण भूमिका निभाते हैं!
एल्कीन (Alkene) असंतृप्त हाइड्रोकार्बन (Unsaturated Hydrocarbon) होते हैं, जिनमें कम से कम एक कार्बन-कार्बन डबल (C=C) बंध मौजूद होता है। इनका सामान्य सूत्र CₙH₂ₙ होता है। एल्कीन का नामकरण IUPAC नियमों के अनुसार किया जाता है, और इनके नाम के अंत में “-ene” (ईन) प्रत्यय जोड़ा जाता है।
एल्कीन (Alkene) कार्बन परमाणु कार्बन परमाणु उपसर्ग तालिका:
| N. | उपसर्ग (Prefix) | हिंदी | उदाहरण (Example – Alkene) | संरचना (Formula) |
|---|---|---|---|---|
| 2 | Eth- | एथ- | Ethene (एथीन) | C₂H₄ |
| 3 | Prop- | प्रोप- | Propene (प्रोपीन) | C₃H₆ |
| 4 | But- | ब्यूट- | Butene (ब्यूटीन) | C₄H₈ |
| 5 | Pent- | पेंट- | Pentene (पेंटीन) | C₅H₁₀ |
| 6 | Hex- | हेक्स- | Hexene (हेक्सीन) | C₆H₁₂ |
| 7 | Hept- | हेप्ट- | Heptene (हेप्टीन) | C₇H₁₄ |
| 8 | Oct- | ऑक्ट- | Octene (ऑक्टीन) | C₈H₁₆ |
| 9 | Non- | नॉन- | Nonene (नॉनिन) | C₉H₁₈ |
| 10 | Dec- | डेक- | Decene (डेकीन) | C₁₀H₂₀ |
| 11 | Undec- | अनडेक- | Undecene (अनडेकीन) | C₁₁H₂₂ |
| 12 | Dodec- | डोडेक- | Dodecene (डोडेकीन) | C₁₂H₂₄ |
| 13 | Tridec- | ट्राइडेक- | Tridecene (ट्राइडेकीन) | C₁₃H₂₆ |
| 14 | Tetradec- | टेट्राडेक- | Tetradecene (टेट्राडेकीन) | C₁₄H₂₈ |
| 15 | Pentadec- | पेंटाडेक- | Pentadecene (पेंटाडेकीन) | C₁₅H₃₀ |
| 16 | Hexadec- | हेक्साडेक- | Hexadecene (हेक्साडेकीन) | C₁₆H₃₂ |
| 17 | Heptadec- | हेप्टाडेक- | Heptadecene (हेप्टाडेकीन) | C₁₇H₃₄ |
| 18 | Octadec- | ऑक्टाडेक- | Octadecene (ऑक्टाडेकीन) | C₁₈H₃₆ |
| 19 | Nonadec- | नोनाडेक- | Nonadecene (नोनाडेकीन) | C₁₉H₃₈ |
| 20 | Icos- | आईकोस- | Icosene (आईकोसीन) | C₂₀H₄₀ |
| 21 | Henicos- | हेनिकोज- | Henicosene (हेनिकोज़ीन) | C₂₁H₄₂ |
| 22 | Docos- | डोकोस- | Docosene (डोकोसीन) | C₂₂H₄₄ |
| 23 | Tricos- | ट्राईकोस- | Tricosene (ट्राईकोसीन) | C₂₃H₄₆ |
| 24 | Tetracos- | टेट्राकोस- | Tetracosene (टेट्राकोसीन) | C₂₄H₄₈ |
| 25 | Pentacos- | पेंटाकोस- | Pentacosene (पेंटाकोसीन) | C₂₅H₅₀ |
| 26 | Hexacos- | हेक्साकोस- | Hexacosene (हेक्साकोसीन) | C₂₆H₅₂ |
| 27 | Heptacos- | हेप्टाकोस- | Heptacosene (हेप्टाकोसीन) | C₂₇H₅₄ |
| 28 | Octacos- | ऑक्टाकोस- | Octacosene (ऑक्टाकोसीन) | C₂₈H₅₆ |
| 29 | Nonacos- | नोनाकोस- | Nonacosene (नोनाकोसीन) | C₂₉H₅₈ |
| 30 | Triacont- | ट्रायाकोंट- | Triacontene (ट्रायाकोंटीन) | C₃₀H₆₀ |
एल्कीन (Alkene) के उदाहरण
- Ethene (एथीन) – C₂H₄
- Propene (प्रोपीन) – C₃H₆
- Butene (ब्यूटीन) – C₄H₈
- Pentene (पेंटीन) – C₅H₁₀
- Hexene (हेक्सीन) – C₆H₁₂
- Heptene (हेप्टीन) – C₇H₁₄
- Octene (ऑक्टीन) – C₈H₁₆
- Nonene (नॉनिन) – C₉H₁₈
- Decene (डेसिन) – C₁₀H₂₀
एल्काइन (Alkyne)
एल्काइन (Alkyne) असंतृप्त हाइड्रोकार्बन (Unsaturated Hydrocarbon) होते हैं, जिनमें कम से कम एक कार्बन-कार्बन ट्रिपल (C≡C) बंध मौजूद होता है। इनका सामान्य सूत्र CₙH₂ₙ₋₂ होता है। एल्काइन का नामकरण IUPAC नियमों के अनुसार किया जाता है, और इनके नाम के अंत में “-yne” (आइन) प्रत्यय जोड़ा जाता है।
- संरचना: एल्काइन में कम से कम एक C≡C (ट्रिपल बंध) होता है।
- सूत्र: CₙH₂ₙ₋₂ फॉर्मूले का पालन करता है।
- प्रतिक्रियाशीलता: एल्कीन से अधिक प्रतिक्रियाशील होते हैं, संयोजन (Addition) प्रतिक्रियाओं में भाग लेते हैं।
- IUPAC नामकरण: नाम के अंत में “-yne” प्रत्यय जोड़ा जाता है।
एल्काइन औद्योगिक रसायन, वेल्डिंग (Acetylene Gas), ईंधन, और जैव रसायन के निर्माण में महत्वपूर्ण भूमिका निभाते हैं!
एल्काइन (Alkyne) कार्बन परमाणु कार्बन परमाणु उपसर्ग तालिका:
| N. | उपसर्ग (Prefix) | हिंदी | उदाहरण (Example – Alkyne) | संरचना (Formula) |
|---|---|---|---|---|
| 2 | Eth- | एथ- | Ethyne (एथाइन) / Acetylene | C₂H₂ |
| 3 | Prop- | प्रोप- | Propyne (प्रोपाइन) | C₃H₄ |
| 4 | But- | ब्यूट- | Butyne (ब्यूटाइन) | C₄H₆ |
| 5 | Pent- | पेंट- | Pentyne (पेंटाइन) | C₅H₈ |
| 6 | Hex- | हेक्स- | Hexyne (हेक्साइन) | C₆H₁₀ |
| 7 | Hept- | हेप्ट- | Heptyne (हेप्टाइन) | C₇H₁₂ |
| 8 | Oct- | ऑक्ट- | Octyne (ऑक्टाइन) | C₈H₁₄ |
| 9 | Non- | नॉन- | Nonyne (नॉनाइन) | C₉H₁₆ |
| 10 | Dec- | डेक- | Decyne (डेकाइन) | C₁₀H₁₈ |
| 11 | Undec- | अनडेक- | Undecyne (अनडेकाइन) | C₁₁H₂₀ |
| 12 | Dodec- | डोडेक- | Dodecyne (डोडेकाइन) | C₁₂H₂₂ |
| 13 | Tridec- | ट्राइडेक- | Tridecyne (ट्राइडेकाइन) | C₁₃H₂₄ |
| 14 | Tetradec- | टेट्राडेक- | Tetradecyne (टेट्राडेकाइन) | C₁₄H₂₆ |
| 15 | Pentadec- | पेंटाडेक- | Pentadecyne (पेंटाडेकाइन) | C₁₅H₂₈ |
| 16 | Hexadec- | हेक्साडेक- | Hexadecyne (हेक्साडेकाइन) | C₁₆H₃₀ |
| 17 | Heptadec- | हेप्टाडेक- | Heptadecyne (हेप्टाडेकाइन) | C₁₇H₃₂ |
| 18 | Octadec- | ऑक्टाडेक- | Octadecyne (ऑक्टाडेकाइन) | C₁₈H₃₄ |
| 19 | Nonadec- | नोनाडेक- | Nonadecyne (नोनाडेकाइन) | C₁₉H₃₆ |
| 20 | Icos- | आईकोस- | Icosaeyne (आईकोसाइन) | C₂₀H₃₈ |
| 21 | Henicos- | हेनिकोज- | Henicosyne (हेनिकोज़ाइन) | C₂₁H₄₀ |
| 22 | Docos- | डोकोस- | Docosyne (डोकोसाइन) | C₂₂H₄₂ |
| 23 | Tricos- | ट्राईकोस- | Tricosyne (ट्राईकोसाइन) | C₂₃H₄₄ |
| 24 | Tetracos- | टेट्राकोस- | Tetracosyne (टेट्राकोसाइन) | C₂₄H₄₆ |
| 25 | Pentacos- | पेंटाकोस- | Pentacosyne (पेंटाकोसाइन) | C₂₅H₄₈ |
| 26 | Hexacos- | हेक्साकोस- | Hexacosyne (हेक्साकोसाइन) | C₂₆H₅₀ |
| 27 | Heptacos- | हेप्टाकोस- | Heptacosyne (हेप्टाकोसाइन) | C₂₇H₅₂ |
| 28 | Octacos- | ऑक्टाकोस- | Octacosyne (ऑक्टाकोसाइन) | C₂₈H₅₄ |
| 29 | Nonacos- | नोनाकोस- | Nonacosyne (नोनाकोसाइन) | C₂₉H₅₆ |
| 30 | Triacont- | ट्रायाकोंट- | Triacontyne (ट्रायाकोंटाइन) | C₃₀H₅₈ |
एल्काइन (Alkyne) के उदाहरण
- Ethyne (एसीटिलीन) – C₂H₂
- Propyne (प्रोपाइन) – C₃H₄
- Butyne (ब्यूटाइन) – C₄H₆
- Pentyne (पेंटाइन) – C₅H₈
- Hexyne (हेक्साइन) – C₆H₁₀
- Heptyne (हेप्टाइन) – C₇H₁₂
- Octyne (ऑक्टाइन) – C₈H₁₄
- Nonyne (नॉनाइन) – C₉H₁₆
- Decyne (डेकाइन) – C₁₀H₁₈
नीचे 50 महत्वपूर्ण रासायनिक यौगिकों के IUPAC नाम, सामान्य नाम, और रासायनिक सूत्र दिए गए हैं:
| N. | IUPAC नाम (हिंदी में) | IUPAC नाम (अंग्रेज़ी में) | सामान्य नाम | रासायनिक सूत्र |
|---|---|---|---|---|
| 1. | डाइहाइड्रोजन मोनोऑक्साइड | Dihydrogen Monoxide | पानी | H₂O |
| 2. | सोडियम क्लोराइड | Sodium Chloride | साधारण नमक | NaCl |
| 3. | सल्फ्यूरिक अम्ल | Sulfuric Acid | गंधक का तेजाब | H₂SO₄ |
| 4. | सोडियम हाइड्रॉक्साइड | Sodium Hydroxide | कास्टिक सोडा | NaOH |
| 5. | हाइड्रोक्लोरिक अम्ल | Hydrochloric Acid | हाइड्रोक्लोरिक एसिड | HCl |
| 6. | नाइट्रोजन ट्राइहाइड्राइड | Nitrogen Trihydride | अमोनिया | NH₃ |
| 7. | कार्बन डाइऑक्साइड | Carbon Dioxide | कार्बन डाइऑक्साइड | CO₂ |
| 8. | मीथेन | Methane | मीथेन | CH₄ |
| 9. | सोडियम कार्बोनेट | Sodium Carbonate | वॉशिंग सोडा | Na₂CO₃ |
| 10. | कैल्शियम ऑक्साइड | Calcium Oxide | बुझा चूना | CaO |
| 11. | नाइट्रिक अम्ल | Nitric Acid | नाइट्रिक एसिड | HNO₃ |
| 12. | पोटैशियम नाइट्रेट | Potassium Nitrate | शोऱा | KNO₃ |
| 13. | ग्लूकोज़ | Glucose | अंगूर की शक्कर | C₆H₁₂O₆ |
| 14. | एथेनोइक अम्ल | Ethanoic Acid | सिरका | CH₃COOH |
| 15. | कैल्शियम कार्बोनेट | Calcium Carbonate | चूना पत्थर | CaCO₃ |
| 16. | एल्यूमिनियम ऑक्साइड | Aluminium Oxide | एलुमिना | Al₂O₃ |
| 17. | आयरन (III) ऑक्साइड | Iron (III) Oxide | हेमेटाइट | Fe₂O₃ |
| 18. | सिल्वर नाइट्रेट | Silver Nitrate | चांदी का नाइट्रेट | AgNO₃ |
| 19. | पोटैशियम क्लोराइड | Potassium Chloride | पोटैशियम क्लोराइड | KCl |
| 20. | मैग्नीशियम सल्फेट | Magnesium Sulfate | एप्सम साल्ट | MgSO₄ |
| 21. | जिंक ऑक्साइड | Zinc Oxide | जस्ता का ऑक्साइड | ZnO |
| 22. | सोडियम बाइकार्बोनेट | Sodium Bicarbonate | बेकिंग सोडा | NaHCO₃ |
| 23. | हाइड्रोजन सल्फाइड | Hydrogen Sulfide | हाइड्रोजन सल्फाइड | H₂S |
| 24. | कॉपर (II) सल्फेट | Copper (II) Sulfate | नीला थोथा | CuSO₄ |
| 25. | टेट्राक्लोरोमीथेन | Tetrachloromethane | कार्बन टेट्राक्लोराइड | CCl₄ |
| 26. | पोटैशियम सल्फेट | Potassium Sulfate | पोटैशियम सल्फेट | K₂SO₄ |
| 27. | बेरियम क्लोराइड | Barium Chloride | बेरियम क्लोराइड | BaCl₂ |
| 28. | आयरन (II) सल्फेट | Iron (II) Sulfate | हरा कसीस | FeSO₄ |
| 29. | अमोनियम क्लोराइड | Ammonium Chloride | नौसादर | NH₄Cl |
| 30. | कॉपर (II) क्लोराइड | Copper (II) Chloride | कॉपर क्लोराइड | CuCl₂ |
| 31. | लिथियम हाइड्रॉक्साइड | Lithium Hydroxide | लिथियम हाइड्रॉक्साइड | LiOH |
| 32. | हाइड्रोजन पेरॉक्साइड | Hydrogen Peroxide | हाइड्रोजन पेरॉक्साइड | H₂O₂ |
| 33. | मेथनॉल | Methanol | मेथनॉल | CH₃OH |
| 34. | एथेनॉल | Ethanol | एथिल अल्कोहल | C₂H₅OH |
| 35. | सोडियम सल्फेट | Sodium Sulfate | सोडियम सल्फेट | Na₂SO₄ |
| 36. | पोटैशियम डाइक्रोमेट | Potassium Dichromate | पोटैशियम डाइक्रोमेट | K₂Cr₂O₇ |
| 37. | फॉस्फोरिक अम्ल | Phosphoric Acid | फॉस्फोरिक एसिड | H₃PO₄ |
| 38. | सोडियम नाइट्रेट | Sodium Nitrate | सोडियम नाइट्रेट | NaNO₃ |
| 39. | पोटैशियम ऑक्साइड | Potassium Oxide | पोटैशियम ऑक्साइड | K₂O |
| 40. | कैल्शियम हाइड्रॉक्साइड | Calcium Hydroxide | बुझा चूना | Ca(OH)₂ |
| 41. | एल्यूमिनियम क्लोराइड | Aluminium Chloride | एल्यूमिनियम क्लोराइड | AlCl₃ |
| 42. | अमोनियम सल्फेट | Ammonium Sulfate | अमोनियम सल्फेट | (NH₄)₂SO₄ |
| 43. | सिलिकॉन डाइऑक्साइड | Silicon Dioxide | सिलिका | SiO₂ |
| 44. | सोडियम सल्फाइड | Sodium Sulfide | सोडियम सल्फाइड | Na₂S |
| 45. | सल्फर डाइऑक्साइड | Sulfur Dioxide | सल्फर डाइऑक्साइड | SO₂ |
| 46. | सोडियम डाइक्रोमेट | Sodium Dichromate | सोडियम डाइक्रोमेट | Na₂Cr₂O₇ |
| 47. | ब्यूटेन | Butane | ब्यूटेन | C₄H₁₀ |
| 48. | पेंटेन | Pentane | पेंटेन | C₅H₁₂ |
| 49. | हेक्सेन | Hexane | हेक्सेन | C₆H₁₄ |
| 50. | हेप्टेन | Heptane | हेप्टेन | C₇H₁₆ |
| 51. | ऑक्टेन | Octane | ऑक्टेन | C₈H₁₈ |
IUPAC नामकरण में संख्या (Numerical Prefixes) का महत्व
IUPAC में संख्यात्मक प्रत्यय (Numerical Prefixes) का उपयोग यह बताने के लिए किया जाता है कि किसी यौगिक में कितने परमाणु या समूह हैं। कुछ प्रमुख प्रत्यय नीचे दिए गए हैं:
| संख्या | IUPAC प्रत्यय | उदाहरण |
|---|---|---|
| 1 | Mono- | Carbon Monoxide (CO) |
| 2 | Di- | Carbon Dioxide (CO₂) |
| 3 | Tri- | Nitrogen Trichloride (NCl₃) |
| 4 | Tetra- | Tetrachloromethane (CCl₄) |
| 5 | Penta- | Phosphorus Pentachloride (PCl₅) |
| 6 | Hexa- | Sulfur Hexafluoride (SF₆) |
| 7 | Hepta- | Heptane (C₇H₁₆) |
| 8 | Octa- | Octane (C₈H₁₈) |
रासायनिक यौगिकों के नामकरण (Nomenclature) और उनके IUPAC नाम प्रतियोगी परीक्षाओं जैसे UPSC, SSC, Railway, Banking, NDA, CDS, AFCAT, NEET, JEE, और State PSC आदि में महत्वपूर्ण भूमिका निभाते हैं। यह विषय विज्ञान के मूलभूत सिद्धांतों को समझने, रासायनिक अभिक्रियाओं (Chemical Reactions) को पहचानने और औद्योगिक व दैनिक जीवन में रसायन विज्ञान के उपयोग को जानने में मदद करता है।
खासकर, NEET और JEE जैसी विज्ञान आधारित परीक्षाओं के लिए यह विषय आवश्यक है, जबकि SSC, UPSC और रेलवे परीक्षाओं में भी इससे जुड़े प्रश्न पूछे जाते हैं। सही IUPAC नाम और रासायनिक सूत्र जानना छात्रों, प्रतियोगी परीक्षार्थियों और विज्ञान में रुचि रखने वालों के लिए बेहद उपयोगी है।
FAQs
महत्वपूर्ण IUPAC नाम लिखो?
- HCl → Hydrochloric Acid (हाइड्रोक्लोरिक अम्ल)
- H₂SO₄ → Sulfuric Acid (गंधक का तेज़ाब)
- NaOH → Sodium Hydroxide (कास्टिक सोडा)
- CH₃COOH → Ethanoic Acid (सिरका/एसिटिक एसिड)
- C₆H₆ → Benzene (बेंजीन)
IUPAC नाम कैसे बनता है?
IUPAC नामकरण में मुख्य श्रृंखला (Longest Chain) चुनने के बाद, संख्या, उपसर्ग (Prefix), मूल समूह (Functional Group), और प्रत्यय (Suffix) को सही क्रम में रखा जाता है। नामकरण के नियम इस प्रकार हैं:
- सबसे लंबी कार्बन श्रृंखला चुनें।
- मुख्य कार्यात्मक समूह (Functional Group) की पहचान करें और उसे सर्वोच्च प्राथमिकता दें।
- संख्या (Numbering) इस तरह करें कि मुख्य कार्यात्मक समूह को सबसे छोटा नंबर मिले।
- शाखाओं (Branches) या उपसमूहों (Substituents) के नाम पहले रखें और उन्हें वर्णानुक्रम में (Alphabetical Order) व्यवस्थित करें।
उदाहरण: CH₃CH₂OH → Ethanol (एथेनॉल)
IUPAC नाम और सामान्य नाम में क्या अंतर है?
- IUPAC नाम वैज्ञानिकों द्वारा निर्धारित एक मानकीकृत (Standardized) नाम होता है, जो वैश्विक रूप से एक ही रहता है।
- सामान्य नाम (Common Name) विभिन्न क्षेत्रों और भाषाओं में अलग-अलग हो सकता है।
उदाहरण:
- H₂O → IUPAC नाम: Dihydrogen Monoxide, सामान्य नाम: पानी
- NaHCO₃ → IUPAC नाम: Sodium Bicarbonate, सामान्य नाम: बेकिंग सोडा